Effect&Efficacy
シモンコライトの多角的抗菌メカニズム
2025.10.31

第1章はじめに:現代社会が求める
新たな抗菌ソリューション
私たちの生活は、見えない微生物との絶え間ない戦いの歴史でした。感染症の脅威、日々の衛生管理、そして身近な体臭や生乾き臭といった不快なニオイ。これらを解決するため、人類は長らく、微生物を徹底的に「殺菌」するアプローチに依存してきました。しかし、その強力さがゆえに、新たな課題も生じています。一部の微生物は特定の薬剤に対して驚くべき速さで耐性を獲得し、「多剤耐性菌」という新たな脅威を生み出しているのです。これは、従来の「根絶」一辺倒の戦略が限界に達しつつあることを示唆しています。また、多くの抗菌剤が生体毒性や環境への影響を懸念される中で、私たちは、微生物を力ずくで排除するのではなく、彼らと賢く共存する、より安全で、効果が持続する根本的なソリューションを求めているのです。
古くから抗菌作用が知られる亜鉛も、その効果を安定して発揮させることは容易ではありませんでした。多くの亜鉛化合物は、水中で亜鉛イオン(Zn2+)を急速に放出し、効果が一時的で不安定になりがちです。また、消臭、吸着、抗菌など、複数の機能を同時に、かつ長期的に持続できる素材は、これまでほとんど存在しませんでした。
テイカ製薬株式会社は、このような時代の要請に応えるべく、多機能性素材としてのシモンコライトの可能性に早くから着目し、長年にわたる研究を鋭意進めてきました。その結果、シモンコライトは、そのユニークな層状構造から、悪臭の吸着、化学反応による消臭、そして微生物の増殖を抑制する抗菌作用という、複数の機能を同時に発揮する画期的な素材であることが明らかになってきたのです1)。
本稿では、シモンコライトが微生物に対してどのように作用するのか、その科学的なメカニズムを深く掘り下げます。シモンコライトは、微生物を単に死滅させるのではなく、その増殖や活動を制御することで、耐性菌の出現リスクを低減し、生態系のバランスを保ちながら衛生状態を維持するという、より高度で持続可能なアプローチを体現していると言えます。これは、単なる抗菌素材の紹介ではなく、科学的根拠に基づいた革新的なアプローチで、未来の衛生・健康社会を築く、新たな哲学の物語なのです。
第2章シモンコライトとは何か?
そのユニークな構造と組成
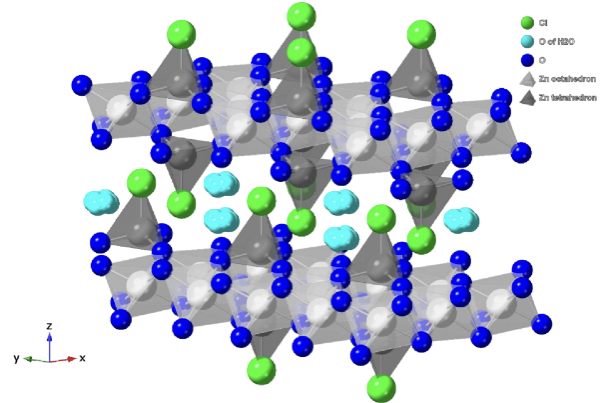
シモンコライトは、化学式Zn5(OH)8Cl2・H2Oで表される塩基性塩化亜鉛であり、自然界に存在する鉱物としても知られています。この物質が他の亜鉛化合物や抗菌素材と一線を画す最大の特長は、その特殊な「層状構造」にあります。シモンコライトは、原子が二次元的なシート状に配列し、その層が比較的弱い力で積み重なった結晶構造を有しています。
この層状構造は、シモンコライトの機能性において極めて重要な役割を果たしています。第一に、この多孔質で層の間に空間を持つ構造は、悪臭成分などの分子を物理的に吸着する能力を可能にします。この吸着能力は、活性炭やゼオライトといった一般的な吸着剤と同様の物理的消臭メカニズムを担います。
しかし、シモンコライトの真価は、その物理構造が、化学的な機能、特に「亜鉛イオン(Zn2+)の徐放性」という全く異なる機能の土台となっている点にあります。層状構造は、亜鉛イオンを安定的に結晶内に保持する「ナノスケールの貯蔵庫」として機能します。この構造がなければ、亜鉛イオンは水溶液中で急速に溶出し、効果は一時的なものにとどまるでしょう。しかし、シモンコライトの層状構造は、水分や外部環境の変化に応じて、亜鉛イオンを徐々に、そして持続的に放出することを可能にします。この徐放性によって、長期間にわたる安定した抗菌・消臭効果が実現されるのです。
このように、シモンコライトのユニークな物理構造は、単なる物理的な吸着機能だけでなく、化学的・生物的な複合機能を可能にしており、この複合性こそが、シモンコライトを次世代型の機能性素材たらしめる所以です。
第3章シモンコライトが微生物に作用する
多角的メカニズム
シモンコライトの抗菌作用は、単一のメカニズムに依存しているのではなく、そのユニークな構造から生み出される複数のメカニズムが同時に作用し、相乗効果を発揮することで実現されています。本稿では、その主要なメカニズムを3つの側面から詳細に解説します。
3.1. メカニズム1:亜鉛イオンによる細胞機能阻害
シモンコライトの層状構造から徐々に放出される亜鉛イオン(Zn2+)は、微生物に直接的に作用する最も基本的なメカニズムの一つです。微生物は、生存に不可欠な微量ミネラルとして亜鉛を取り込むための輸送体を持っています。シモンコライトから放出された「亜鉛イオン」は、この輸送体を通じて細胞内に取り込まれますが、過剰な量が細胞内に蓄積することで、生命維持に不可欠な機能が阻害されます。
詳細な作用機序としては、細胞内に過剰に取り込まれた「亜鉛イオン」は、微生物の生存に不可欠なタンパク質の立体構造を変化させ、また、酵素の活性部位に結合してその機能を阻害します。例えば、細菌のDNA複製や転写に関わる酵素(ポリメラーゼなど)の機能を妨害し、微生物の増殖そのものを停止させます。さらに、亜鉛イオンは細胞壁の分解酵素であるペプチドグリカン(PGN)オートリシンを活性化させ、細菌の細胞壁を破壊して細胞死を誘発する「バクテリオライシス」を引き起こすことも報告されています。
研究では、シモンコライトが黄色ブドウ球菌(Staphylococcus aureus)や大腸菌(Escherichia coli)といった主要な病原菌の増殖を、添加量に依存して抑制することが示されています3)。
このメカニズムは、微生物の代謝活動を根本から阻害することで、持続的な抗菌効果をもたらします。
3.2. メカニズム2:バイオフィルム形成の強力な抑制
近年、医療分野や工業分野で大きな課題となっているのが「バイオフィルム」です。バイオフィルムとは、細菌が互いに協力して形成する集合体であり、その強固な保護マトリックス(多糖類やタンパク質)によって、抗生物質や消毒剤が届きにくく、感染症の難治化や製品の劣化を引き起こす原因となります。
塩化亜鉛や硫酸亜鉛のような亜鉛塩が、高濃度ではバイオフィルム形成を抑制するものの、低濃度ではかえって細菌のストレス応答を引き起こし、バイオフィルム形成を促進させてしまうことが知られています。これは、微生物が生存戦略として、金属ストレスから身を守るためにバイオフィルムを強化するためです。
しかし、シモンコライトは、このバイオフィルム形成を効果的に抑制するという、極めて重要な機能を有しています。特筆すべきは、他の亜鉛化合物とは異なり、バイオフィルム形成を抑制するのに十分な抗菌作用を持つ「最小発育阻止濃度」以下(subinhibitory concentrations)の低濃度でも、バイオフィルムの形成を効果的に阻害することが確認されている点です4)。この作用は、微生物が物体表面に付着する初期段階を妨げることで、バイオフィルム形成のライフサイクルの最も早い段階に作用するため、非常に効率的なアプローチと言えます。実際に、特に難治性の感染症の原因菌として知られる緑膿菌(Pseudomonas aeruginosa)に対し、約90%のバイオフィルム形成抑制効果が確認されています5)。
この特性は、シモンコライトが微生物のストレス応答を誘発することなく、根本的な増殖制御を可能にするという、シモンコライトの優位性を示しています。
3.3. メカニズム3:亜鉛イオンと光活性による活性酸素種(ROS)の生成
シモンコライトは、その電気化学的性質に由来する複数の経路を通じて、微生物の細胞に酸化ストレスを引き起こす「活性酸素種」(ROS: Reactive Oxygen Species)を生成することが報告されています4)。このROS生成メカニズムは、主に以下の2つの経路が考えられます。
1) シモンコライト表面でのROS生成
シモンコライトは、半導体酸化亜鉛(ZnO)粉末の製造段階で生成する中間体粉末であり、ZnOと同様に、ワイドバンドギャップ(~3.33 eV)を持つ半導体としての性質を有しています。このため、光、特に紫外線(UV)を照射されると、その表面で電子(e–)と正孔(h+)のペアが生成されると考えられます。この正孔(h+)は、表面に吸着した水分子や水酸基(OH–)と反応して非常に反応性の高いヒドロキシラジカル(•OH)を生成し、電子(e–)は酸素分子(O₂)と反応してスーパーオキシドアニオン(•O₂–)を形成します。これらのROSは、微生物の細胞膜、脂質、タンパク質、そしてDNAを酸化させ、細胞機能に致命的なダメージを与えます。
なお、シモンコライト単独でもこの特性はありますが、シモンコライトとZnOの複合体は、より優れた光触媒活性と高いROS生成能力を示すことが報告されています。
2) 細胞内での亜鉛イオンによるROS生成
シモンコライトの層状構造から徐々に放出され、細胞内に取り込まれた亜鉛イオン(Zn2+)が、直接的にROS生成を誘発する経路も報告されています。細胞内の亜鉛濃度が過剰になると、特にミトコンドリアに流入した「亜鉛イオン」が、活性酸素種の生成を急速に引き起こすことが知られています。これにより、微生物は内部から酸化ストレスを受け、細胞の機能不全や細胞死に至ります。
3.4. 多角的メカニズムによる相乗効果
これらのメカニズムは独立して働くのではなく、微生物の増殖の異なる段階に同時に作用することで、相乗的な抗菌効果を生み出していると考えられます。例えば、まず、シモンコライトから徐々に放出される低濃度の「亜鉛イオン」がバイオフィルム形成を阻害し、さらに高濃度では直接的な細胞機能阻害やROS生成による殺菌効果を発揮するといった、濃度依存的・段階的な作用が推測できます。
この多角的なアプローチは、微生物に特定の耐性メカニズムを発達させる機会を与えにくく、持続的な抗菌効果を保証する上で極めて有利な特性です。
第4章研究事例で見る
シモンコライトの抗菌スペクトル
シモンコライトの抗菌作用は、これまでの研究を通じて、多岐にわたる微生物に対して有効であることがデータで裏付けられています。特に、日常生活における衛生課題の原因となる微生物から、医療や公衆衛生上重要な病原菌、さらには真菌類に至るまで、広範な抗菌スペクトルを有することが確認されています。
4.1. 皮膚常在菌と真菌に対する有効性
頭皮のフケやかゆみ、体臭や加齢臭は、皮膚の常在菌であるコリネバクテリウム属細菌や、真菌であるマラセチア属真菌が、汗や皮脂を分解することで発生します。テイカ製薬株式会社の研究では、微粒子化したシモンコライトがこれらの微生物の増殖を効果的に抑制することが見出されました。
具体的には、寒天希釈法を用いた実験において、わずか0.02%という低濃度でコリネバクテリウムの増殖を完全に抑制し、0.1%の濃度でマラセチアの増殖を完全に抑制するデータが得られています6)。また、シモンコライトがモラクセラ属細菌に対しても抗菌作用を有することが確認されており7)、頭皮環境の改善に多角的に貢献することが期待されます。この結果は、ごく少量で優れた効果を発揮するため、頭皮ケアやスキンケア製品への応用が極めて理にかなっていることを示しています。
4.2. 主要な病原菌と真菌に対する抗菌活性
公衆衛生の観点から重要な病原菌に対するシモンコライトの有効性も確認されています。以下の表に、主要な微生物に対するシモンコライトの抗菌活性データを示します。
| 微生物名 | 試験方法 | 結果 | 参考資料 |
黄色ブドウ球菌(Staphylococcus aureus ATCC 25,923) | ディスク拡散法 | 阻止円(10 mg/mL): 10.7 mm | 5) |
大腸菌(Escherichia coli O157:H7) | ディスク拡散法 | 阻止円(10 mg/mL): 10.7 mm | 5) |
緑膿菌(Pseudomonas aeruginosa ATCC 27,853) | バイオフィルム形成抑制試験 | 73%(5 mg/mL)、89%(10 mg/mL)抑制 | 5) |
カンジダ(Candida albicans NBRC 1594) | 日本薬局方準拠 | 抗菌効果あり | 7) |
クロコウジカビ(Aspergillus brasiliensis NRBC 9455) | 日本薬局方準拠 | 抗菌効果あり | 7) |
コリネバクテリウム(Corynebacterium striatus NBRC 15291) | 寒天希釈法 | 0.02%で完全増殖抑制 | 7) |
マラセチア(Malassetia furfur BNRC 10987) | 寒天希釈法 | 0.1%で完全増殖抑制 | 7) |
このデータは、シモンコライトがグラム陽性菌、グラム陰性菌、そして真菌類に至るまで、広範な微生物に対して有効であることを明確に示しています。特に、バイオフィルム形成の抑制効果は、抗生物質耐性菌の問題が深刻化する中で、シモンコライトが新たな感染症対策の鍵となりうる可能性を示唆しています。専門家や開発者にとって、感覚的な「効果がある」という表現ではなく、このような具体的な数値データは、シモンコライトの優位性を論理的に構築する上で不可欠な要素です。
4.3. 抗菌活性の定量的評価(MIC)
研究では、シモンコライトの抗菌効果を定量的に評価するため、最小発育阻止濃度(MIC: Minimum Inhibitory Concentration)という指標が用いられています。これは、微生物の増殖を完全に抑制するために必要な最小の抗菌剤濃度を示すもので、数値が低いほど強力な抗菌作用を持つことを意味します。シモンコライトは、例えば、黄色ブドウ球菌やコリネバクテリウム属細菌に対し、MIC値が200 µg/mL未満と判定され、優れた抗菌効果を有することが確認されています7)。このデータは、シモンコライトが非常に少量でも効果を発揮する、高効率な素材であることを裏付けています。
4.4. 複合体としての相乗効果
シモンコライトは、他の物質と組み合わせることで、その抗菌性能をさらに高めることが報告されています。例えば、シモンコライトに植物由来の抗菌成分であるチモールを吸着させた複合体(ナノハイブリッド)は、単独のシモンコライトよりも優れた抗菌作用を示し、黄色ブドウ球菌および大腸菌O157:H7に対して、それぞれ24 mmおよび21 mmの阻止円を形成することが確認されています5)(シモンコライト単独では、いずれも10.7 mmの阻止円を形成)。さらに、この複合体は、難治性感染症の原因菌である緑膿菌のバイオフィルム形成を、5 mg/mLで86%、10 mg/mLで92%抑制する効果も見出されています。
第5章抗菌作用がもたらす
革新的な応用分野
シモンコライトの多角的な抗菌メカニズムと広範な抗菌スペクトルは、様々な産業分野に革新をもたらす可能性を秘めています。
5.1. 頭皮ケア・スキンケア製品
体臭や頭皮の臭いは、汗や皮脂が微生物によって分解されることで発生するものです。従来の消臭剤が臭い分子を吸着したり中和したりするのに対し、シモンコライトは、臭いの「発生源」である微生物の増殖を根本から抑制する「抗菌防臭」作用を有しています。ナノ粒子化されたシモンコライトは、地肌である頭皮の角質層のすみずみまで浸透し、臭いやフケ、かゆみの原因となるコリネバクテリウムやマラセチアといった微生物の増殖を制御します7)。これにより、単なる一時的なマスキングや消臭ではなく、根本的な頭皮環境の改善をもたらす新たなソリューションとなります。
5.2. 繊維・紙製品
現代社会では、日用品に抗菌機能が付与されることが一般的になっています。シモンコライトは、その優れた抗菌・防カビ特性から、繊維や紙製品への応用も進められています。研究結果では、紙や布にシモンコライトを含有(付着)させることで、容易に抗菌製品が得られることが確認されています7)。また、シモンコライトは吸着した悪臭成分を再放散させることがほとんどないため、加工された製品に長期的な抗菌・防臭効果を付与することが可能になります。これにより、医療現場の衛生用品から、一般消費者の日用品まで、幅広い分野でシモンコライトが安全かつ持続的な抗菌機能を提供できることが示されています。
5.3. 医療分野(生体材料・コーティング)
医療機器、特にインプラントやカテーテルなどでは、微生物の付着によるバイオフィルム形成が感染症の主要な原因となっており、抗菌性と生体適合性の両立が大きな課題でした。シモンコライトは、生体適合性が高く、栄養飼料添加物としても使用される安全な素材でありながら、優れた抗菌作用を示します。
さらに、シモンコライトが、ZnOよりも毒性が低く、生体適合性が高いことから、シモンコライトとZnOナノ結晶の複合体は、ZnO単体よりも生体適合性が飛躍的に向上しつつ抗菌効果を維持できることが報告されています4)。この事実は、医療機器へのコーティング剤としての可能性を強く示唆しています。これは、抗生物質に代わる新たな感染症対策として、未来の医療技術に貢献する極めて重要な知見と言えます。
第6章まとめ:複合的な機能を持つ
次世代の抗菌素材
本稿で詳述したように、シモンコライトの抗菌作用は、単なる亜鉛イオンの作用にとどまらず、複数のメカニズムが協働する複合的なものです。具体的には、その層状構造から徐々に放出される亜鉛イオン(Zn2+)による細胞機能阻害、他の亜鉛化合物とは異なり低濃度でもバイオフィルム形成を抑制する特異的な能力、そして電気化学的活性に起因する活性酸素種(ROS)の生成による酸化ストレスが、その多角的な抗菌作用を構成しています。
シモンコライトの核心的な価値は、「安全性」「持続性」「多機能性」という3つの特性に集約されます。栄養飼料添加物としても使用される高い生体適合性は、様々な製品への応用における安全性の基盤となります。また、その層状構造に由来する亜鉛イオンの徐放性は、効果の持続性を保証します。そして、物理的な吸着(消臭)、化学的な反応(消臭)、生物的な作用(抗菌)という複合機能は、他の単機能素材との決定的な違いであり、これを自然由来で実現している点がシモンコライトの優位性を確立しています。
シモンコライトは、単なる消臭剤でも、単なる抗菌剤でもありません。臭いの根本原因である微生物の活動を抑制し、人体や環境に優しく、持続的な効果を発揮する次世代の機能性素材です。その多角的でユニークな特性は、今後、医療、美容、衛生用品、環境技術など、未開拓の分野で更なる応用研究が進むことが期待されます。シモンコライトは、科学的根拠に基づいた革新的なアプローチで、未来の衛生・健康社会を築く上で不可欠な存在となるでしょう。
参考資料
1) 学術的研究 – シモンコライト研究所(https://simonkolleite.jp/academic-research/)
2) Qu, S.; Hadjittofis, E.; Malaret, F.; Hallett, J.; Smith, R.; Campbell, K.S. Nanoscale Adv., 2023, DOI:10.1039/D3NA00108C
3) Li, S.; Chen, X.; Wang, X.; Xiong, Y.; Yan, Y.; Tan, Z.; Yang, X.; Li, Y. Polymers, 2019;11, 1505
4) Oliveira, J.M.; Costa, M.P.C.; Perini, H.F.; Trevisan, R.O.; Almeida, L.I.M.; Matos, S.L.M.; Sousa, I.O.F.; Ruiz, L.C.; Silva, L.E.A.; Rodrigues, V. Jr.; Oliveira, C.J.F.; Silva, M.V.; Anhezini, L.; Silva, A.C.A. ACS Omega, 2025;10, 20117
5) Velázquez-Carriles, C.; Macías-Rodríguez, M.E.; Ramírez-Alvarado, O.; Corona-González, R.I.; Macías-Lamas, A.; García-Vera, I.; Cavazos-Garduño, A.; Villagrán, Z.; Silva-Jara, J.M. Molecules, 2022;27, 6161
6) 薄毛と菌の関係性とは?シモンコライトの菌に対する効果 – シモンコライト研究所(https://simonkolleite.jp/bacteria/)
7) 国際公開2024/224747 「抗菌剤」