Effect&Efficacy
亜鉛不足が招く味覚障害の全貌
2025.10.31
――メカニズムから最新治療、臨床統計まで

第1章はじめに:QOL向上に欠かせない味覚の重要性
1.1. 現代における味覚障害への関心の高まり
「最近、味がしない」――。夕飯の食卓で、いつもより調味料に手が伸びる。好物の出汁の香りに心が動かない。みそ汁が妙に“平板”に感じられ、甘いはずの果物がぼんやりする。最初は「風邪気味かな」「年齢のせいかな」と見過ごしがちですが、こうした細かな違和感が積み重なると、食べる喜びそのものが薄れていきます。味覚は生命維持に直結しないからこそ軽視されやすいのですが、単なる生存だけでなく、生活の質(Quality of Life, QOL)を支える重要な感覚の一つです。近年、医療の進歩により健康寿命が延伸される中、日々の食生活の満足度を著しく低下させる味覚障害は、その原因究明と適切な治療が極めて重要なテーマとして、関心が高まっています。
1.2. 新型コロナウイルス感染症と味覚・嗅覚障害
2020年初頭に世界的に流行が始まった新型コロナウイルス感染症(COVID-19)の初期には、急性発症の味覚・嗅覚障害が特徴的な症状として広く認識されました。しかし、2023年7月時点では、その発症率は激減しています。
COVID-19後の味覚障害の病態は未だ不明な点が多いものの、神経細胞の障害が主な原因であると示唆されています。これは、亜鉛欠乏による味蕾の代謝障害とは異なるメカニズムであると考えられます。一方で、COVID-19罹患による食欲不振や偏食が、間接的に亜鉛不足を引き起こし、それが味覚障害を悪化させたり、新たな味覚障害の原因となったりする可能性も指摘されています。したがって、COVID-19後の味覚障害に対する亜鉛補充療法は、ウイルスの直接的な影響を治療するものではなく、感染を契機として生じた二次的な亜鉛欠乏状態を是正することで、味覚機能の改善を図る合理的なアプローチであると解釈されています。
第2章亜鉛の基礎知識:生命活動を支える必須微量元素
2.1. 亜鉛の体内における働きと役割
亜鉛は、ヒトの体内に約2g含まれる必須微量元素であり、そのほとんどは筋肉と骨に存在しますが、皮膚、肝臓、脾臓、前立腺など、多くの臓器に広く分布しています。亜鉛は、200種類以上の酵素の構成要素として、細胞の新陳代謝、特にタンパク質やDNAの合成に不可欠な役割を担っています。亜鉛が不足すると、これらの重要な生体機能が阻害されるため、成長遅延、免疫機能の低下、皮膚炎、脱毛、性腺発達障害など、全身に多岐にわたる症状が発現します。
2.2. 日本人の亜鉛食事摂取基準(2025年版
食事から摂取された亜鉛の吸収率は、同時に摂取される他の成分によって変動しますが、一般的には約30%と推定されています。厚生労働省が定める「日本人の食事摂取基準(2025年版)」では、亜鉛の1日の推奨摂取量が年齢や性別ごとに細かく設定されています。この基準は、読者が自身の食生活を評価し、亜鉛不足のリスクを認識する上で非常に有用な情報となります。
| 性別 | 年齢区分 | 1日あたりの推奨量(mg) |
| 男性 | 18~29歳 | 9.0 |
| 30~64歳 | 9.5 | |
| 65歳以上 | 9.0 | |
| 女性 | 18~29歳 | 7.5 |
| 30~64歳 | 8.0 | |
| 65~74歳 | 7.5 | |
| 75歳以上 | 7.0 |
亜鉛が豊富な食品としては、牡蠣、煮干し、豚レバー、牛赤身肉、カシューナッツ、きな粉などが挙げられます。これらの食品をバランス良く摂取することが、亜鉛不足の予防に繋がります。
第3章味覚のメカニズムと亜鉛の役割:多層的な貢献
3.1. 味覚の基礎:五基本味と味蕾の構造
味覚は、甘味、塩味、酸味、苦味、旨味の5つの基本味から構成される化学感覚です。これらの味は、舌の表面にある小さな突起(舌乳頭)に存在する「味蕾(みらい)」と呼ばれる器官の、さらに内部にある「味細胞」が、食品中の化学物質を受容することで生じます。味細胞は、約2週間という非常に速いサイクルで新陳代謝を繰り返しており、常に新しい細胞に置き換わっています。味覚の受容や伝達は、味細胞から味神経を介して脳に伝えられる一連のプロセスであり、亜鉛欠乏によりこの経路の末梢部で障害が生じると、味神経の電気信号にも変化が起こると考えられています。
3.2. 亜鉛が味覚を司る多層的なメカニズム
亜鉛が味覚機能に果たす役割は、単一の作用ではなく、細胞の代謝から神経の伝達に至るまで、複数の階層にわたる複合的なものです。
まず、亜鉛は味細胞の産生に必須であり、DNAやタンパク質の合成を担うDNAポリメラーゼやRNAポリメラーゼといった200種類以上もの酵素の構成要素となっています。亜鉛が欠乏すると、これらの重要な生体機能が阻害されるため、味蕾のターンオーバー(新陳代謝)の周期が延長します。その結果、機能が低下した古い味細胞が舌の表面を占める割合が増え、味の認識能力が低下します。この細胞レベルの障害は、舌乳頭の扁平化や味細胞の表面にある微絨毛の消失といった形態学的異常として現れることが報告されています。さらに、味覚障害患者の舌の顕微鏡画像では、健常者の舌に比べて舌乳頭への血管の流入が途絶え、血行が不良であることが示されています(後述)。これは、細胞再生の遅延と血行不良が互いに影響し合い、味覚機能の低下を加速させる複合的な病態であることを示唆しています。
加えて、亜鉛は味覚神経の反応を円滑にする上で重要な役割を担っています。味蕾に多く存在する炭酸脱水酵素は、亜鉛を必須とする酵素であり、その活性が低下すると味覚神経の反応が悪くなると考えられています。亜鉛欠乏ラットを用いた研究では、亜鉛不足が舌に分布する三叉神経や鼓索神経の反応低下をもたらすことが示されており、受容体(味蕾・味細胞)だけでなく、神経レベルでも亜鉛が重要な役割を果たすことが明らかになっています。
3.3. 最新研究が解き明かす分子メカニズム:亜鉛の新規役割
従来の「構造的・代謝的役割」という理解を超え、近年の研究は、亜鉛が味覚シグナル伝達においてより能動的で直接的な役割を担っている可能性を示唆しています。これは、亜鉛が単なる味細胞の「構成要素」ではなく、味覚の「情報伝達物質」として機能するという、役割のパラダイムシフトを提示するものです。
味覚情報伝達における亜鉛の新規役割:神経伝達物質としての機能1)
亜鉛は、中枢神経系(特に海馬)において、神経伝達物質として機能することが広く知られています。味覚細胞においても同様のメカニズムが存在する可能性が、最新の研究で明らかになりつつあります。特定の味覚細胞(II型細胞とIII型細胞)に発現する亜鉛トランスポーターであるZnT3が、亜鉛を前シナプス小胞内に蓄積します。味覚刺激を受けた味細胞は、これらの小胞から細胞間隙に亜鉛を放出し、この放出された亜鉛が味蕾内のシグナル伝達を調節している可能性が示唆されています。この知見は、亜鉛補充療法が単に細胞の再生を促すだけでなく、既存のシグナル伝達経路を直接的に改善する即効的な効果も持ちうるという可能性を示唆するものです。
特定の味覚(特に甘味)に対する亜鉛の抑制作用2)
亜鉛の味覚への影響は、「回復」だけにとどまりません。最新の研究は、亜鉛が甘味の知覚を約75%抑制する可能性を示唆しています。この発見は、亜鉛が味覚障害の治療という文脈を超え、肥満やメタボリックシンドロームの主要因である糖分の過剰摂取を抑制するための、新たな栄養学的・薬理学的アプローチとして応用される可能性を秘めているものです。
参考資料
1)Nishida, K.; Bansho, S.; Ikukawa, A.; Kubota, T.; Ohishi, A.; Nagasawa, K. Eur. J. Histochem., 2022;66, 3534
2)University of Nebraska-Lincoln, Office of Research and InnovationのWEB サイト(https://research.unl.edu/blog/sukumaran-seeks-to-better-understand-zincs-role-in-taste/)
第4章亜鉛欠乏性味覚障害:その病態と原因の分類
4.1. 多岐にわたる味覚障害の原因
味覚障害の原因は非常に多様であり、その病態や頻度は年齢によっても大きく異なります。主要な原因としては、他の疾患治療のために服用する薬剤の副作用(薬剤性味覚障害)、原因が特定できない突発性味覚障害、亜鉛の代謝に関与する全身性疾患(慢性肝疾患、糖尿病、腎不全など)、口腔内の乾燥を伴う疾患などが挙げられます。
薬剤性味覚障害:
薬剤が原因で引き起こされる味覚障害は、味覚障害全体の24%を占めており、特に70歳以上の高齢者では約35%が薬剤性であると報告されています。薬剤が味覚に影響を及ぼすメカニズムは、主に3つに分類されます。1つ目は、ペニシラミンなどの薬剤が亜鉛と結合してキレートを形成し、亜鉛の吸収を阻害・排泄を亢進することで亜鉛欠乏を引き起こすというものです。2つ目は、抗コリン作用を持つ薬剤が唾液分泌を抑制し、味物質が味蕾に到達するのを妨げるというものです。3つ目は、味覚情報を脳に伝える味覚神経に直接影響を与えるケースです。薬剤性味覚障害の治療においては、原因薬剤の中止、減量、または他の薬剤への変更が検討されます。また、血清亜鉛値が正常であっても、組織内の亜鉛濃度が低い場合があるため、亜鉛製剤の補給が治療法として考慮されます。治療効果は、発症から治療開始までの期間が短いほど高いため、早期の診断と治療が非常に重要です。
全身性疾患:
慢性肝疾患、糖尿病、慢性腎臓病などの全身性疾患も、亜鉛欠乏を伴うことで味覚障害の原因となります。
- 慢性肝疾患: 慢性肝炎や肝硬変の患者では、食事からの亜鉛吸収率の低下と尿中への亜鉛排泄の亢進により、亜鉛欠乏状態に陥りやすいことが知られています。また、アルコール摂取は肝臓の亜鉛バランスを乱し、細胞内の亜鉛不足を引き起こす可能性があります。
- 糖尿病: 亜鉛は、インスリンの構成成分であり、その合成・貯蔵・分泌に関与する重要な役割を担っています。そのため、亜鉛が不足するとインスリンの分泌が減少し、血糖値の上昇を招くと言われています。
- 慢性腎臓病(CKD): 慢性腎臓病の患者では、尿からの亜鉛の排泄が増加することが近年明らかになっています。特に、GFR(糸球体濾過量)が低下するほど亜鉛の排出は急激に増加し、亜鉛欠乏がCKD進行の危険因子となることも報告されています。
口腔・唾液腺疾患:
味覚障害を訴える患者の94%に、口腔内の乾燥や痛みといった口腔症状がみられると報告されています。このうち、最も高頻度な原因は唾液分泌量の減少によって引き起こされるドライマウス(口腔乾燥症)です。唾液には、味物質を味蕾に運搬し、味覚を感じやすくする重要な働きがあります。唾液の分泌は自律神経によって調節されており、自律神経の乱れや、特定の薬剤の副作用などが原因で唾液分泌が減少すると、味覚障害を引き起こす可能性があります。
4.2. 亜鉛欠乏症の診断基準と臨床的課題
亜鉛欠乏症の診断は、主に血清亜鉛値に基づいて行われます。しかし、その基準値には複数の定義が存在するため、臨床的判断を複雑にしているのが現状です。一般的に、血清亜鉛値が60 μg/dL未満を「亜鉛欠乏症」、60~80 μg/dL未満を「潜在性亜鉛欠乏症」として区別しています。
軽度から中等度の亜鉛欠乏は血清検査では検出されない場合もあるため、診断は単に血清値に依存するものではありません。症状(皮膚炎、味覚障害など)、血清アルカリホスファターゼ(ALP)値の低下、そして亜鉛補充療法による症状の改善効果などを総合的に判断する必要があります。したがって、味覚障害の診断は単純な検査結果の読み取りではなく、鑑別診断が重要となります。これは、亜鉛欠乏と類似した症状を引き起こす他の疾患(鉄欠乏、ビタミンB12欠乏、グルカゴノーマ、うつ病など)との見極めが不可欠であることを意味します。
表1:味覚障害の診断における血清亜鉛値の基準と解釈
| 基準の名称 | 血清亜鉛値 | 定義 | 備考/補足 |
| 日本臨床栄養学会 | <60 μg/dL | 亜鉛欠乏症 | 症状、ALP値、治療反応性と組み合わせて判断 |
| 日本臨床栄養学会 | 60~80 μg/dL未満 | 潜在性亜鉛欠乏 | 症状、ALP値、治療反応性と組み合わせて判断 |
| 臨床診療における参考値 | <80 μg/dL | 亜鉛欠乏性味覚障害 | 潜在的亜鉛欠乏が疑われる特発性味覚障害を含む |
| 臨床統計による考察 | ≤70 μg/dL | 亜鉛不足の傾向 | 鉄欠乏性、心因性、外傷性を除く味覚障害の原因の50~70%を占める |
| 原因分類 | 亜鉛補充療法の適応 |
| 亜鉛欠乏性味覚障害 | 主要な治療法として投与 |
| 突発性味覚障害 | 潜在的な亜鉛欠乏が疑われるため投与 |
| 薬剤性味覚障害 | 服用薬剤の調整と並行して投与を検討 |
| 全身性疾患に伴う味覚障害 | 原疾患の治療と並行して投与 |
| 口腔・唾液腺疾患に伴う味覚障害 | 口腔内乾燥症治療薬などと並行して投与を検討 |
第5章兵庫医科大学臨床統計に見る亜鉛欠乏性味覚障害の実態
5.1. 1000例を超える症例の分析1)
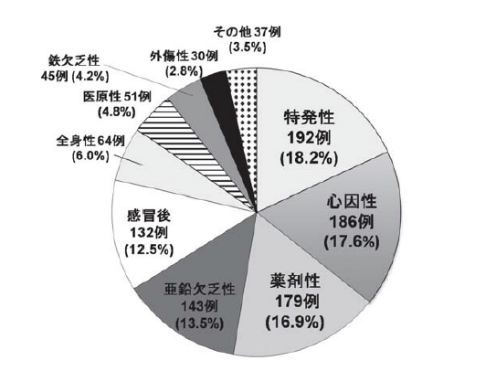
兵庫医科大学耳鼻咽喉科が1999年から2010年にかけて実施した、1059例を対象とした大規模な臨床統計は、亜鉛欠乏性味覚障害の実態を明らかにする貴重なデータを提供しています 。この統計によると、味覚障害の原因のうち、特発性と亜鉛欠乏症が合わせて30%強を占めており、その関与の大きさが示唆されました。
[試験概要]
| 評価期間 | 1999年1月から2010年12月 |
| 対象者 | 1059例(男性412例、女性647例)12歳から89歳 |
| 検査・評価項目 | 前例初診時問診・電気味覚検査・自覚症状評価・味覚乳頭観察など |
5.2. 舌乳頭の形態学的変化:健常者と患者の比較1)
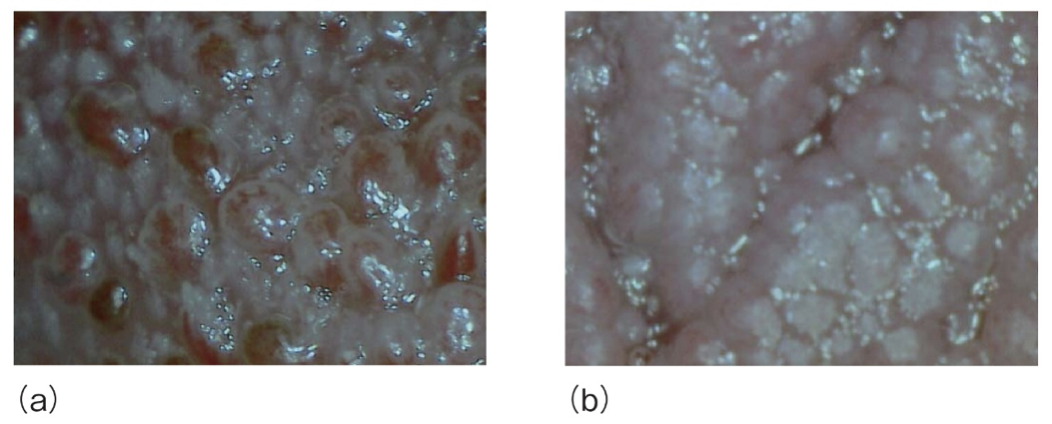
この研究では、マイクロスコープを用いた舌の観察も行われました。その結果、健常人の舌では舌乳頭への血管の流入が良好である一方(a)、味覚障害患者の舌では血管の途絶が見られ、その走行も不明瞭であることが確認されました(b)。この形態学的変化は、亜鉛欠乏が味細胞の代謝だけでなく、舌の微小循環にも影響を及ぼしている可能性を示唆しています。
5.3. 量的異常と質的異常の分類から見る新たな知見2)
兵庫医科大学の別の報告では、亜鉛欠乏性・特発性味覚障害患者を「味が薄く感じる量的異常」と「味が変に感じる質的異常」に分類して比較検討が行われました。この研究によると、質的異常の患者は量的異常の患者に比べて年齢層が有意に高く、血清亜鉛値が正常範囲内である例が多かったことが明らかになりました。
この事実は、単に血清亜鉛値が正常範囲内であるからといって、亜鉛が味覚障害に関与していないとは断定できないことを示しています。質的異常の患者においては、亜鉛の量的欠乏というよりは、加齢や特定の疾患など、亜鉛の代謝や体内での利用効率に問題がある可能性、あるいは味覚情報伝達経路のより高次な中枢神経系に問題がある可能性が示唆されます。この知見は、亜鉛欠乏性味覚障害の診断と治療が、単なる血清亜鉛値の測定だけでなく、患者の症状、年齢、併存疾患、服用薬剤などを総合的に考慮する多角的なアプローチを必要とすることを強く示唆しています。
参考資料
1)任智美、阪上雅史.亜鉛栄養治療、2012;2、46
2)西井智子、任智美、梅本匡則、前田英美、阪上雅史.口咽科、2018;31、131
第6章亜鉛補充療法:確立された治療法とその詳細
6.1. 治療の原則と対象
現在、味覚障害に対して確立された治療法は亜鉛補充療法のみとされており、その有効性は多くの臨床報告によって裏付けられています。亜鉛補充療法は、血清亜鉛値が80 μg/dL未満である亜鉛欠乏性味覚障害の主要な治療法として推奨されています。また、血清亜鉛値が正常であっても、他の原因が特定できず潜在的な亜鉛欠乏が疑われる突発性味覚障害の患者に対しても、主要な治療法として投与が行われることが一般的です。さらに、服用薬剤の調整が難しい薬剤性味覚障害や、全身性疾患に伴う味覚障害に対しても、原疾患の治療と並行して亜鉛製剤の投与が行われます。治療効果を最大限に高めるためには、発症から治療開始までの期間が短いほど有効率が高まるため、早期の診断と治療が非常に重要であると指摘されています。
6.2. 亜鉛補充療法の詳細と投与管理
投与量と治療期間:
亜鉛補充療法により、味蕾細胞の再生が促進され、味覚障害が改善したという報告があります。具体的な投与量については、成人で亜鉛として1日あたり50~100 mgを、通常1日2回に分けて食後に経口投与することが治療指針で示されています。小児の場合には、体重に応じて1~3 mg/kg/日または体重20 kg未満で25 mg/日、20kg以上で50 mg/日を分割投与します。治療効果を実感するまでには時間を要し、4~6カ月にわたる長期的な補給が必要となる場合もありますが、中には亜鉛補充療法を開始したことで、速やかに自覚症状が改善した症例も報告されています。
安全管理と注意点:
亜鉛補充療法においては、治療の有効性だけでなく、安全な管理が非常に重要です。過剰な亜鉛の投与は、体内の銅や鉄の吸収を阻害し、欠乏を招くリスクがあるだけでなく、膵酵素の上昇を引き起こす可能性も指摘されています。このため、治療中は数カ月に一度、血清亜鉛、銅、鉄の値を定期的に測定することが推奨されています。血清亜鉛値が250 μg/dL以上になった場合は、投与量を減量する必要があります。このような定期的なモニタリングは、安全かつ効果的な治療管理に不可欠であり、専門的な医療機関での指導のもとに行われるべきです。
主な亜鉛製剤:
亜鉛補充療法に用いられる製剤としては、ポラプレジンク製剤と酢酸亜鉛製剤の2種類が存在します。これらの製剤は、患者の症状や体質に合わせて使い分けられることがあります。例えば、ある症例では、亜鉛欠乏性味覚障害と診断され酢酸亜鉛水和物の投与を開始したところ、消化器症状を認めたため、ポラプレジンクに変更して治療を継続し、味覚障害と低亜鉛血症の改善を認めたという報告があります。
COVID-19後の味覚障害への適用:
新型コロナウイルス感染症後の味覚障害には、現時点で確立された治療法は存在しません。しかし、発症から2週間以内に60~80%が自然に改善すると報告されており、症状が長引く場合は、亜鉛や漢方薬による治療が試みられることがあります。COVID-19罹患による食欲不振や偏食が間接的に亜鉛不足を引き起こし、味覚障害を悪化させたり、新たな原因となったりする可能性が指摘されているため、亜鉛補充療法は、ウイルスの直接的な影響を治療するのではなく、二次的に生じた亜鉛欠乏状態を是正する合理的なアプローチであると解釈されています。2023年に中国から報告された論文によると、オミクロン株以降の罹患者の40%以上が、口の中に苦みを感じる、何を食べてもまずい味がするなどの特異な症状を訴えていることが明らかになっています。また、COVID-19罹患者は低亜鉛血症になりやすく、唾液中の亜鉛濃度も著しく低い傾向があることが報告されており、味覚障害からの回復とともに亜鉛値も回復するケースがあることも指摘されています。
| 対象となる味覚障害の病態 | 研究の概要 | 治療効果の有無/結果 |
| 特発性、慢性腎不全 | 2023年発表のメタ分析 | 有効性が確認された |
| COVID-19後遺症 | 観察研究 | 100 mg/日を4~6ヶ月間の補給で改善報告あり |
| 化学療法に伴う味覚障害 | 複数のRCT | プラセボとの有意差は認められず、有効性は示されていない |
| 消化管術後 | 観察研究 | 亜鉛の有効率は高いが、原疾患のコントロールも不可欠 |
6.3. 亜鉛補充療法以外の治療法と併用療法の重要性
味覚障害の治療は、単一の亜鉛補充に限定されるべきではなく、原因に応じた多角的なアプローチが求められます。治療期間は、症状の改善までに最低3~6ヶ月かかるのが一般的であり、発症から6ヶ月以上経過すると改善率が有意に低下し、治療期間も長期化する傾向があるため、早期の治療が非常に重要です。
- 原因薬剤の調整:薬剤性味覚障害の場合、原因薬剤の減量、中止、または代替薬への変更が最も根本的な治療となります。
- 口腔・唾液腺疾患の治療:口腔内の乾燥が味覚障害の原因となることが多いため、唾液腺マッサージや人工唾液の処方、口腔内ケアが有効です。
- 漢方薬・生薬:安全性の高い治療法として、当帰芍薬散、加味帰脾湯、人参養栄湯などが使用されることがあります。
- 精神的サポート:味覚障害は、うつ病や心因性のものである場合があるため、抗うつ薬や抗不安薬による治療、および心理的サポートが不可欠です。味覚や嗅覚の喪失が、視力喪失よりも深刻な心理的影響を与えるという指摘もあります。
- その他の栄養療法:亜鉛欠乏症との鑑別診断の観点から、ビタミンB12、α-リポ酸、ビタミンD、鉄分などの補充が有効な場合があることも報告されています。
第7章亜鉛の栄養学的管理と生活習慣の改善
7.1. 食事からの亜鉛摂取:吸収を促進・阻害する要因
亜鉛の不足は、食事からの摂取不足が主要な原因の一つです。効果的な亜鉛摂取のためには、吸収を促進する食品と阻害する食品の組み合わせを理解することが重要となります。
- 吸収を促進する要因:
- クエン酸:酢、梅干し、柑橘類に多く含まれ、亜鉛と結合して吸収しやすい形に変えます。
- ビタミンC:トマト、ピーマン、カボチャ、レモンなどの野菜や果物に豊富であり、亜鉛の吸収を高めます。
- 動物性タンパク質:肉類、魚介類、乳製品などに含まれる動物性タンパク質は、亜鉛の吸収効率を上げます。
- 吸収を阻害する要因:
- フィチン酸:未精製の穀物や豆類(大豆、玄米)に多く含まれ、亜鉛と結合して吸収を妨げます。
- 食物繊維:野菜、海藻、キノコなど、多くの植物性食品に含まれます。
- タンニン:緑茶、コーヒー、紅茶、渋柿などに含まれます。
- ポリリン酸:加工食品に多く含まれます。
- アルコール:亜鉛の排泄を増加させるため、過度な飲酒は避けるべきです。
単純に「亜鉛を多く含む食品を摂る」という指導だけでは不十分であり、他の栄養素や食品との組み合わせに配慮した、より実践的な食生活指導が重要です。例えば、亜鉛を多く含む大豆や玄米は、同時に吸収を阻害するフィチン酸も含むため、ビタミンCやクエン酸を同時に摂取する工夫が有効です。
7.2. 亜鉛サプリメントの賢い選び方と注意点
食事からの十分な摂取が困難な場合は、サプリメントの活用も有効な選択肢となります。その際には、以下の点に注意が必要です。
- 適切な含有量:亜鉛の目標摂取量は1日あたり30 mgとされており、過剰摂取は銅欠乏症などを引き起こす可能性があるため、特に高用量の海外製品には注意が必要です。
- 吸収性を考慮した配合:ビタミンCやクエン酸が同時に配合されている製品は、吸収効率が高いため推奨されます。
- 形態の選択:タブレット、カプセル、グミなど様々な形態があります。服用しやすさで選ぶべきですが、グミタイプは糖分や添加物が多い場合があるため注意が必要です。
- 品質保証の確認:長期的に摂取する場合は、製造管理体制が厳格に管理された製品(GMP認証など)を選択することが重要です。
第8章まとめと今後の展望
本稿では、亜鉛不足が引き起こす味覚障害について、その発症メカニズムから、臨床における実態、確立された治療法に至るまで、多角的に考察しました。
亜鉛は、味蕾細胞の再生、酵素活性の維持、そして神経伝達の円滑化という、味覚システムの複数の階層にわたる重要な役割を担っています。特に、味覚シグナル伝達における能動的な神経伝達物質としての新規な役割が示唆され、その重要性は再定義されつつあります。また、甘味の知覚を抑制するという新たな発見は、亜鉛が味覚障害の治療だけでなく、肥満やメタボリックシンドロームの予防・管理に貢献する可能性を示しています。
味覚障害の原因は多岐にわたりますが、亜鉛欠乏は最も一般的な原因の一つであり、特に原因不明とされてきた突発性味覚障害の中にも、潜在的な亜鉛不足が深く関与していることが明らかになっています。味覚障害の診断は、血清亜鉛値のみに依存するものではなく、全身性疾患や薬剤性など多岐にわたる原因を考慮した包括的な鑑別診断が不可欠です。
亜鉛補充療法は現時点で最も確立された治療法であり、適切な投与量と期間、そして定期的なモニタリングを通じて、多くの患者のQOL向上に貢献しています。しかし、特定の病態(例:化学療法に伴うもの)には有効性が示されていないなど、病態に応じた治療法の選択が重要です。治療は、亜鉛補充に加えて、原因薬剤の調整や心理的サポートを含む多角的なアプローチが求められます。
今後の展望として、味覚障害の多様な病態、特に血清亜鉛値が正常な症例における亜鉛の関与や、COVID-19後の味覚障害の神経学的メカニズムについてのさらなる研究が期待されます。これらの知見は、個々の患者の味覚障害の原因に合わせた個別化医療の発展に寄与するでしょう。さらに、味覚障害が精神的ウェルビーイングに与える深刻な影響を考慮し、診療における心理的サポートの重要性も再認識されるべきです。これらの課題を解決するためには、味覚障害に関する系統立てられた診療ガイドラインの作成も不可欠です。
従来の「構造的・代謝的役割」という理解を超え、近年の研究は、亜鉛が味覚シグナル伝達においてより能動的で直接的な役割を担っている可能性を示唆しています。これは、亜鉛が単なる味細胞の「構成要素」ではなく、味覚の「情報伝達物質」として機能するという、役割のパラダイムシフトを提示するものです。
味覚情報伝達における亜鉛の新規役割:神経伝達物質としての機能1)
亜鉛は、中枢神経系(特に海馬)において、神経伝達物質として機能することが広く知られています。味覚細胞においても同様のメカニズムが存在する可能性が、最新の研究で明らかになりつつあります。特定の味覚細胞(II型細胞とIII型細胞)に発現する亜鉛トランスポーターであるZnT3が、亜鉛を前シナプス小胞内に蓄積します。味覚刺激を受けた味細胞は、これらの小胞から細胞間隙に亜鉛を放出し、この放出された亜鉛が味蕾内のシグナル伝達を調節している可能性が示唆されています。この知見は、亜鉛補充療法が単に細胞の再生を促すだけでなく、既存のシグナル伝達経路を直接的に改善する即効的な効果も持ちうるという可能性を示唆するものです。
特定の味覚(特に甘味)に対する亜鉛の抑制作用2)
亜鉛の味覚への影響は、「回復」だけにとどまりません。最新の研究は、亜鉛が甘味の知覚を約75%抑制する可能性を示唆しています。この発見は、亜鉛が味覚障害の治療という文脈を超え、肥満やメタボリックシンドロームの主要因である糖分の過剰摂取を抑制するための、新たな栄養学的・薬理学的アプローチとして応用される可能性を秘めているものです。
次の記事が
ありません。